اپاندیموم گرید ۲ مغز تومورهای نادری هستند که از سلولهای اپاندیمال منشأ میگیرند و نقش مهمی در دستگاه عصبی مرکزی دارند. در طبقهبندی WHO اپاندیمومها به گریدهای متفاوت تقسیم میشوند و گرید II به جهتی “کلاسیک” یا “متوسط” شناخته میشود. در طبقهبندیهای جدید، تمایز بر اساس شاخصهای مولکولی نیز اهمیت بیشتری دارد هرچند هنوز در همه مراکز اعمال نشده است. اپاندیموم گرید II میتواند در نواحی مختلف سیستم عصبی مرکزی (مغز یا نخاع) ایجاد شود. بسته به محل دقیق، علائم و گزینههای درمان متفاوت است.
بالینی و اپیدمیولوژی
- اپاندیمومها در بزرگسالان کمتر از ۲٪ تومورهای مغزی را تشکیل میدهند، اما در کودکان سهم بیشتری دارند.
- در موارد نخاعی (Intramedullary)، تقریبا ۵۵ تا ۷۵٪ تومورهای نخاعی کلاسیک مربوط به گرید II هستند.
- در حالت نخاعی، انواعی چون cellular ependymoma، clear-cell، tanycytic و giant cell وجود دارد که رفتار متفاوتی نشان میدهند.
- در مطالعه Sun و همکاران، آمار نشان داد که بیماران با نوع giant cell ممکن است نتایج بدتری نسبت به نوع cellular داشته باشند.
تشخیص اپاندیموم گرید ۲ مغز
روش های تشخیص این بیماری عبارتند از:
تصویربرداری
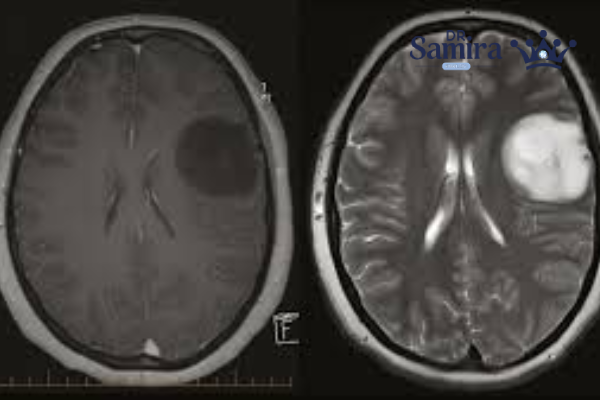
تصویربرداری مغزی و نخاعی با MRI بهترین گزینه برای تشخیص است. این روش میتواند محل، اندازه، ارتباط با بافتهای مجاور و احتمال گسترش را نشان دهد. برای مواردی که تومور واقع در ناحیه مغزی است، پس از جراحی و در پیگیریها نیز MRI دورهای کاربرد دارد. در برخی مطالعات نوظهور، روشهای رادیومیک (Radiomics) و یادگیری ماشینی روی تصاویر MRI برای کمک به درجهبندی تومورها مورد بررسی قرار گرفتهاند. اگرچه بیشتر این مطالعات روی گلیوماها انجام شدهاند نه صرفاً اپاندیموم، میتوان به چشم یک گرایش آیندهنگر نگاه کرد.
بیوپسی و پاتولوژی
تشخیص قطعی وابسته به بررسی بافتی است. در بافتشناسی گرید II، ویژگیهایی مانند pseudorosettes (پزودوروستل) شایع هستند.
همچنین شمارش میتوزها، میزان تکثیر سلولی، نفوذ بافت اطراف و شاخص تقسیم (proliferation index) (مثلاً Ki-67) برای تعیین درجه و پیشبینی رفتار استفاده میشوند. علاوه بر آن، بررسی مایع مغزی-نخاعی (CSF cytology) در مواردی که احتمال انتشار در مایع وجود دارد، ممکن است درخواست شود.
بیشتر بدانید: میکسو پاپیلاری اپاندیمومای نخاع
اصول درمان اپاندیموم گرید ۲ مغز
در درمان اپاندیموم گرید II، چند نکته کلیدی هستند که هنوز بین محققان و مراکز درمان اختلاف نظر وجود دارد. در ادامه با استناد به مقالات معتبر، این بحثها را توضیح میدهم.
جراحی: هدف، میزان برداشت و تاثیر آن
هدف جراحی «برداشت حداکثر امن» است؛ یعنی تا آنجا که میتوان بدون آسیب به ساختارهای حیاتی، تومور را خارج کرد. مطالعات متعدد نشان دادهاند که برداشت کامل (Gross Total Resection, GTR) با بهبود بقا و کاهش احتمال عود همراه است. مثلا در مطالعه چند مرکزی روی بیماران با گرید II، کسانی که جراحی کامل داشتند بقا و کنترل بهتر بیماری را نشان دادند. با این حال، در برخی موارد به دلیل نزدیکی تومور به ساختارهای حیاتی، امکان برداشت کامل وجود ندارد (Subtotal resection, STR). در این مواقع، تصمیمگیری درباره استفاده از پرتودرمانی پساعملی مهم میشود.
در مورد تومورهای نخاعی هم مطالعات نشان میدهند که برداشت بیشتر تومور با نتایج بهتری همراه است، البته باید با احتیاط و با حفظ عملکرد عصبی باشد.
پرتودرمانی پس از جراحی: بین استفاده یا تامل
یکی از بحث برانگیزترین مباحث درمان اپاندیموم گرید II، این است که آیا پس از جراحی (به ویژه وقتی برداشت کامل انجام شده) باید پرتودرمانی انجام شود یا میتوان تحت نظر گرفت.
مثالی از این بحث در مقاله “Do We Need Radiotherapy in Grade II Ependymoma?” مطرح شده است، که نشان میدهد در بیماران با ضایعه مغزی و جراحی غیرکامل، پرتودرمانی ممکن است مزایایی داشته باشد.
در همان مطالعه، در دوره پیگیری، نرخ بقای کلی در ۵ و ۱۰ سال به ترتیب ۸۷٪ و ۸۳٪ گزارش شده است. پرتودرمانی موضعی باعث بهبود بقا بدون پیشرفت (PFS) در برخی موارد شد، بهخصوص در کسانی که برداشت کامل انجام نشده بود.
مطالعه متاآنالیز «Adjuvant radiotherapy versus observation after gross total resection» نیز نشان داد که پرتودرمانی پس از جراحی کامل (GTR) همراه با بهبود معنیدار بقا نیست، اما پس از جراحی ناقص (STR) پرتودرمانی با بقا بهتر همراه بوده است.
در مورد تومورهای داخل نخاعی، مطالعه اخیر “Long-Term Outcomes after Incomplete Resection …” نشان داده است که اگر برداشت ناقص انجام شود، عدم استفاده از پرتودرمانی بهطور سیستماتیک ممکن است گزینهای منطقی باشد، چرا که در بسیاری از بیماران پیشرفت علائم شناسایی نشده و نیاز فوری به درمان بیشتر نبوده است.
مطالعه دیگری با عنوان “Optimizing outcomes in intracranial ependymoma” تاکید میکند که در ضایعات درون مغزی گرید II یا III اگر برداشتن کامل ممکن نباشد، ترکیب جراحی، پرتودرمانی موضعی، و در برخی مواقع شیمیدرمانی ممکن است بهترین استراتژی باشد.
بیشتر بدانید: آستروسیتوم گرید ۳؛ تومور آناپلاستیک مغز
خلاصه بحث پرتودرمانی پسا عملی:
- اگر جراحی کامل انجام شود، ممکن است بتوان از پرتودرمانی صرفنظر کرد در موارد خاص، مخصوصا اگر تومور در ناحیه مغزی باشد و خطر عوارض پرتویی زیاد باشد.
- اگر جراحی ناقص بوده باشد (STR)، شواهدی وجود دارد که پرتودرمانی پساعملی میتواند بقا و کنترل محلی را بهبود دهد.
- هنوز شواهد قطعی از مطالعات تصادفی بزرگ وجود ندارد و تصمیمگیری اغلب براساس عوامل فردی (محل تومور، سن بیمار، وضعیت عمومی، خطر عوارض پرتویی) انجام میشود.
شیمی درمانی و درمانهای مکمل
در اپاندیموم گرید ۲ مغز، نقش شیمی درمانی هنوز قطعی نیست و در بیشتر موارد به عنوان درمان کمکی یا پشتیبان در شرایط خاص (مثلا کودکان، موارد مقاوم یا با انتشار) در نظر گرفته میشود. در مقاله «Optimizing outcomes …» ذکر میشود که شیمیدرمانی ممکن است برای تاخیر پرتودرمانی در کودکان زیر یک سال استفاده شود، اما شواهد قوی برای اثبات اثرگذاری آن ندارد. در بسیاری از مراکز، شیمیدرمانی به عنوان درمان نگهدارنده یا در شرایط عود پیشنهاد میشود، اما هنوز استاندارد قطعی نشده است.
عوامل موثر در عود اپاندیموم گرید ۲ مغز
پیشبینی در اپاندیموم گرید II به عوامل گوناگون بستگی دارد. در این بخش، به مرور عوامل موثر خواهیم پرداخت. میزان برداشت جراحی یکی از قویترین پیشبینیکنندههاست. جراحی کامل با نتایج بهتر همراه است. برخی مطالعات نشان دادهاند که تومورهای نخاعی نسبت به ضایعات مغزی ممکن است نتایج بهتری داشته باشند. (یعنی بقا بهتر یا نرخ عود پایینتر) در برخی مطالعات، سن پایینتر یا شرایط ویژه سنی، بهویژه در کودکان خردسال، با نتایج ضعیفتر همراه بوده است.
با پیشرفت علم، دانشمندان به اهمیت ویژگیهای مولکولی تومور (مثل تغییرات ژنتیکی، بیان ژنها، مسیرهای سیگنالدهی سلولی) پی بردهاند که میتواند در پیشبینی رفتار و پاسخ به درمان تعیینکننده باشد. وجود انتشار در مایع مغزی-نخاعی (CSF dissemination) در مواردی که تومور در مایع منتشر شده باشد، خطر عود دور از محل اولیه را بیشتر میکند.
بیشتر بدانید: آستروسیتوم گرید ۴
پیگیری و مراقبت بلند مدت بعد از درمان
یک نکته مهم در مدیریت بیماران مبتلا به اپاندیموم گرید II، اهمیت پیگیری بلندمدت است چون امکان عود حتی پس از سالها وجود دارد.
- بررسی دورهای با MRI هر ۶ ماه تا ۲ سال پس از جراحی، سپس سالانه انجام میشود.
- اگر علائمی جدیدی مانند سردرد، ضعف یا تشنج بروز کند، سریعا باید بررسی شود.
- در مواردی که باقیمانده تومور وجود دارد یا شواهدی از پیشرفت تصویری مشاهده شود، تیم تصمیم به درمان مجدد (جراحی، پرتودرمانی، یا ترکیبی) میگیرد.
- مدیریت عوارض جانبی درمان (مثلا عوارض پرتودرمانی، اختلالات عصبی، مشکلات شناختی) اهمیت زیادی دارد و نیازمند تیم تخصصی (نورولوژیست، روانپزشک، توانبخشی) است.
در مراکز پیشرفته، استفاده از روشهای جدید پرتودرمانی پیشرفته مانند پرتودرمانی پروتونی یا arc therapy ممکن است امکان کاهش عوارض با حفظ اثربخشی را فراهم کند. بهعنوان مثال، در یکی از مطالعات پیشنهاد شده است که Intensity Modulated Proton Arc Therapy (IMPAT) میتواند مزایای دزکنترولی و همگرایی در تومورهای اپاندیمومی داشته باشد.


