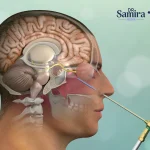
انواع آدنوم هیپوفیز موضوعی مهم در غدد درونریز و نورولوژی است، چون این تومورها با اینکه اغلب خوشخیماند، میتوانند با ترشح نابجای هورمونها یا فشار بر بافتهای اطراف، طیف بزرگی از علائم بالینی ایجاد کنند. آدنوم هیپوفیز به تومورهایی گفته میشود که از سلولهای هیپوفیز قدامی منشأ میگیرند و رشد آهسته دارند. طبقهبندی این آدنومها به چند شکل انجام میشود: بر اساس ترشح هورمون (کارکردی یا غیرکارکردی)، بر اساس نوع سلول سازنده و هورمون غالب، و همچنین بر اساس اندازه و تهاجم به ساختارهای مجاور. در این مقاله، انواع آدنوم هیپوفیز را با نگاه بالینی و پاتولوژیک توضیح میدهیم و ویژگیهای هر گروه را مرور میکنیم.
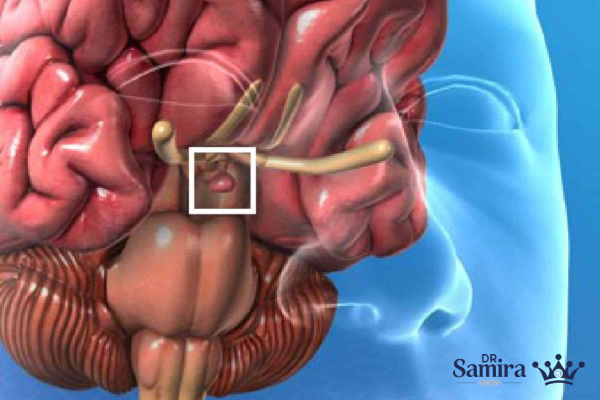
دستهبندی آدنومهای هیپوفیز بر اساس ترشح هورمون
آدنومهای هیپوفیز از نظر ترشح هورمون به کارکردی و غیرکارکردی تقسیم میشوند:
آدنوم هیپوفیز کارکردی چیست و چه علائمی دارد؟
در آدنومهای کارکردی (Functioning)، تومور هورمون فعال ترشح میکند و همین ترشح، علامتهای بالینی ایجاد میکند. در مقابل، آدنومهای غیرکارکردی (Non-functioning) هورمون مؤثر بالینی نمیسازند یا ترشحشان آنقدر کم است که در بدن علامت مشخصی نمیدهد.
آدنوم هیپوفیز غیرکارکردی چیست و چگونه تشخیص داده میشود؟
آدنومهای کارکردی زودتر تشخیص داده میشوند، چون بیمار با شکایتهای هورمونی مراجعه میکند. اما آدنومهای غیرکارکردی غالباً دیرتر و وقتی بزرگ شدهاند کشف میشوند؛ چون نشانههایشان بیشتر «فشاری» است. حدود یکسوم آدنومهای هیپوفیز بهطور بالینی غیرکارکردیاند
بیشتر بدانید: انواع متاستاز به مغز
پرولاکتینوما یا آدنوم پرولاکتینساز هیپوفیز
پرولاکتینوما یا آدنوم لاکتوتروف از سلولهایی منشأ میگیرد که در حالت طبیعی هورمون پرولاکتین میسازند. این نوع، شایعترین آدنوم کارکردی هیپوفیز محسوب میشود. افزایش پرولاکتین در زنان باعث نامنظمی قاعدگی، قطع قاعدگی، ناباروری و گاهی ترشح شیر از پستان (گالاکتوره) میشود. در مردان، تظاهرات بیشتر به صورت کاهش میل جنسی، اختلال نعوظ، ناباروری و در موارد پیشرفته کاهش توده عضلانی یا پوکی استخوان دیده میشود. از نظر درمانی، پرولاکتینوماها به آگونیستهای دوپامین مثل کابرگولین یا بروموکریپتین پاسخ خیلی خوبی میدهند و در بسیاری از بیماران حتی اندازه تومور هم کوچک میشود؛ به همین دلیل درمان دارویی خط اول است.
آدنوم هورمون رشد و ارتباط آن با آکرومگالی و ژیگانتیسم
آدنوم سوماتوتروف باعث ترشح بیش از حد هورمون رشد (GH) میشود. اگر این اتفاق قبل از بسته شدن صفحات رشد استخوانی رخ دهد، بیمار دچار ژیگانتیسم (بلندقدی غیرطبیعی) میشود؛ اما در بزرگسالان باعث آکرومگالی است. آکرومگالی با بزرگ شدن تدریجی دستها و پاها، درشت شدن اجزای صورت، تغییر صدا، تعریق زیاد، درد مفاصل و در بلندمدت افزایش خطر دیابت، پرفشاری خون و بیماریهای قلبی همراه است. تشخیص با بالا بودن IGF-1 و عدم سرکوب GH در تست خوراکی گلوکز انجام میشود و MRI نقش کلیدی در تعیین اندازه و گسترش تومور دارد. درمان غالباً جراحی ترانساسفنوییدال است و در صورت باقیماندن بیماری، از داروهایی مثل آنالوگهای سوماتواستاتین یا آنتاگونیست گیرنده GH استفاده میشود.
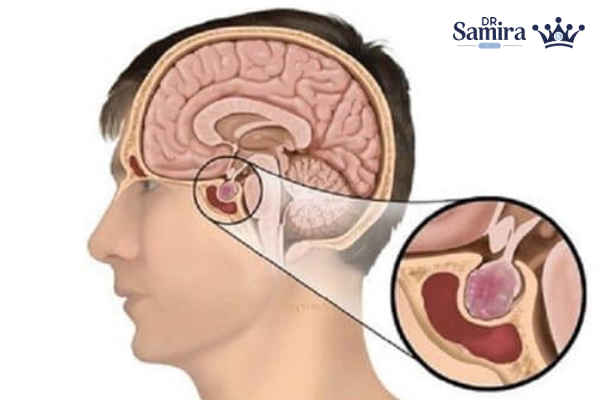
آدنوم ACTHساز هیپوفیز و ایجاد بیماری کوشینگ
در آدنوم کورتیکوتروف، سلولهای سازنده ACTH به شکل خودمختار فعال میشوند و قشر آدرنال را به تولید بیش از حد کورتیزول تحریک میکنند. نتیجهٔ این زنجیره، «بیماری کوشینگ» است. بیماران اصولا با افزایش وزن مرکزی، صورت گرد و پُر («Moon face»)، تجمع چربی پشت گردن، نازکی پوست، کبودی آسان، خطوط پوستی ارغوانی، ضعف عضلانی، فشار خون بالا و گاهی اختلالات روانی مراجعه میکنند. این نوع آدنومها اگرچه ممکن است از نظر اندازه کوچک باشند (اغلب میکروآدنوم)، اما اثر هورمونی بسیار واضحی دارند. درمان استاندارد، جراحی تومور از راه بینی (ترانساسفنوییدال) است و در صورت عدم بهبود کامل، داروهای مهارکنندهٔ سنتز کورتیزول یا پرتودرمانی مطرح میشوند.
آدنوم TSHساز هیپوفیز؛ علت نادر پرکاری تیروئید ثانویه
آدنوم ترشحکنندهٔ هورمون محرک تیروئید (TSH) بسیار کمتر از انواع قبلی دیده میشود، اما از نظر بالینی مهم است چون یک الگوی خاص از پرکاری تیروئید ایجاد میکند: بیمار هم علائم هایپرتیروئیدی دارد (تپش قلب، کاهش وزن، لرزش، تحریکپذیری) و هم در آزمایشها TSH برخلاف پرکاری تیروئید معمولی سرکوب نشده و حتی بالا است. این ویژگی تشخیصی کمک میکند تا این بیماران از پرکاری تیروئید اولیه تفکیک شوند. درمان غالبا شامل جراحی و در صورت نیاز، آنالوگهای سوماتواستاتین برای مهار TSH است.
بیشتر بدانید: مراقبت های بعد از رادیوتراپی
آدنومهای غیرکارکردی و گنادوتروف هیپوفیز
بخش قابل توجهی از آدنومهای هیپوفیز از سلولهای گنادوتروف منشأ میگیرند؛ این سلولها در حالت طبیعی LH و FSH تولید میکنند. با این حال، بسیاری از این تومورها از نظر بالینی «غیرکارکردی» تلقی میشوند چون ترشحشان اثر واضحی در بدن ایجاد نمیکند. بنابراین بیماران بیشتر با علائم ناشی از فشار تومور مراجعه میکنند: سردرد، تاری دید یا از بین رفتن میدان دید طرفی (به علت فشار بر کیاسمای بینایی)، و گاهی کاهش عملکرد سایر هورمونهای هیپوفیز. در MRI اغلب ماکروآدنوم دیده میشود چون این تومورها دیرتر علامتدار میشوند. درمان جراحی است و در موارد باقیمانده یا عود، پرتودرمانی کمککننده است.
انواع آدنوم هیپوفیز بر اساس اندازه تومور
آدنومهای هیپوفیز از نظر اندازه به چند گروه تقسیم میشوند و این تقسیمبندی در تصمیم درمانی و پیشآگهی نقش دارد:
- میکروآدنوم:
قطر کمتر از ۱۰ میلیمتر که معمولا دیرتر باعث اثر فشاری میشود و اگر کارکردی باشد، به دلیل علائم هورمونی زود تشخیص داده میشود. جراحی در صورت نیاز سادهتر است و احتمال آسیب به ساختارهای اطراف کمتر است.
- ماکروآدنوم:
قطر آن ۱۰ میلیمتر یا بیشتر است. بیشتر احتمال دارد به کیاسمای بینایی فشار آورد یا به سینوس کاورنوس گسترش پیدا کند. در این حالت سردرد و اختلال دید شایع است و درمان جراحی پیچیدهتر میشود.
- آدنومهای غولآسا:
در اکثر موارد بزرگتر از ۴ سانتیمتر هستند. اینها میتوانند به شکل تهاجمی به بالا یا طرفین رشد کنند و هم علائم فشاری شدید و هم اختلالهای گسترده هورمونی ایجاد کنند. اغلب نیاز به درمان ترکیبی (جراحی + دارو + پرتودرمانی) دارند.
طبقهبندی جدید WHO برای آدنومهای هیپوفیز بر پایه دودمان سلولی
در طبقهبندیهای جدید، اصطلاح «Pituitary Neuroendocrine Tumor» یا PitNET برای بسیاری از آدنومها به کار میرود تا رفتار بالقوه تهاجمی بعضی از آنها بهتر توضیح داده شود. در این رویکرد، تومورها بر اساس دودمان سلولی و فاکتورهای رونویسی (مثل PIT-1، TPIT و SF-1) دستهبندی میشوند. مثلاً آدنومهای لاکتوتروف و سوماتوتروف در دودمان PIT-1 قرار میگیرند، آدنومهای کورتیکوتروف با TPIT و آدنومهای گنادوتروف با SF-1 شناخته میشوند. این تقسیمبندی پاتولوژیک به پیشبینی رفتار تومور و احتمال عود کمک میکند.
روشهای درمان آدنوم هیپوفیز
درمان آدنوم هیپوفیز ترکیبی و «شخصی سازی شده» است؛ یعنی پزشک با توجه به نوع تومور، اندازه و محل آن، و شدت علائم تصمیم میگیرد. هدفها شامل کنترل ترشح هورمونی، کوچککردن یا برداشتن توده، و پیشگیری از آسیب به بینایی و عملکرد طبیعی هیپوفیز است.
درمان دارویی
در بعضی آدنومها، دارو «خط اول» است و حتی میتواند اندازه تومور را کم کند. مهمترین کاربردش در آدنومهای هورمون ساز است.
پرولاکتینوما:
برای پرولاکتینوماها، داروهای آگونیست دوپامین مثل کابرگولین و بروموکریپتین درمان اصلیاند. این داروها سطح پرولاکتین را پایین میآورند و در بیشتر بیماران، اندازهٔ تومور هم کوچک میشود؛ بنابراین جراحی فقط در موارد مقاوم یا عدم تحمل دارو مطرح است.
آدنوم هورمون رشد (آکرومگالی):
اگر بعد از جراحی ترشح GH/IGF-1 باقی بماند یا بیمار امکان جراحی نداشته باشد، از آنالوگهای سوماتواستاتین (مثل اکتروتاید/لانرئوتاید) یا آنتاگونیست گیرندهٔ GH (پگوویسومانت) استفاده میشود تا هورمون کنترل شود.
آدنوم ACTH-ساز (بیماری کوشینگ):
وقتی جراحی کامل موفق نباشد یا تا زمان اثر پرتودرمانی نیاز به کنترل کورتیزول باشد، داروهای مهارکنندهٔ تولید کورتیزول در آدرنال بهکار میروند. این داروها کمک میکنند علائم کوشینگ کنترل شود.
آدنوم TSH-ساز:
در موارد نادر TSH-ساز، دارو (بهخصوص آنالوگهای سوماتواستاتین) میتواند پرکاری تیروئید و ترشح TSH را کاهش دهد، ولی درمان اصلی جراحی است.
جراحی ترانس اسفنوییدال
جراحی از راه بینی و سینوس اسفنویید درمان استاندارد برای بیشتر آدنومهای هیپوفیز است، مخصوصاً وقتی تومور بزرگ باشد، به عصب بینایی فشار بیاورد، یا ترشح هورمونی شدید و مقاوم ایجاد کند. این روش کمتهاجمیتر از جراحی باز بوده و در دست تیم مجرب، شانس کنترل بیماری بالاست.
چه زمانی جراحی ضروریتر است؟
- ماکروآدنومها یا تودههایی که اختلال میدان دید یا سردرد فشاری ایجاد کنند.
- آدنومهای GH-ساز یا ACTH-ساز که برای «بهبود قطعی» نیاز به برداشت تومور دارند.
پرتودرمانی و رادیوسرجری
پرتودرمانی زمانی استفاده میشود که:
- بعد از جراحی بخشی از تومور باقی بماند،
- تومور عود کند،
- یا بیمار کاندید جراحی نباشد.
دو شکل رایج دارد:
- پرتودرمانی معمولیِ چندجلسهای
- رادیوسرجری استریوتاکتیک (SRS)
بیشتر بدانید: کیست آراکنوئید مغز
درمانهای ویژه برای تومورهای تهاجمی یا مقاوم
در درصد کمی از بیماران، تومور رفتار تهاجمی دارد یا با جراحی/دارو/پرتو کنترل نمیشود. در این حالت، در مراکز تخصصی ممکن است از:
- تموزولوماید یا همان شیمی درمانی انتخابی برای PitNET تهاجمی
- و گاهی درمانهای هدفمند یا کارآزماییهای بالینی جدید
استفاده شود. این گروه نادر است و نیاز به تیم چندتخصصی دارد.
خلاصه مطالب…
آدنومهای هیپوفیز، با وجود خوشخیم بودن در اکثر موارد، از مهمترین تومورهای درونجمجمهای هستند چون میتوانند هم تعادل هورمونی بدن را بههم بزنند و هم با فشار بر ساختارهای حیاتی مغز، علائم عصبی ایجاد کنند. شناخت انواع آدنوم هیپوفیز چه بر اساس ترشح هورمون (کارکردی و غیرکارکردی)، چه بر اساس نوع سلول سازنده و چه بر اساس اندازه به پزشک کمک میکند مسیر تشخیص و درمان را دقیقتر انتخاب کند. پرولاکتینوماها شایعترین نوع کارکردیاند و اغلب با دارو کنترل میشوند، در حالی که آدنومهای سوماتوتروف و کورتیکوتروف بیشتر نیازمند جراحیاند. آدنومهای غیرکارکردی و گنادوتروف دیرتر و با علائم فشاری دیده میشوند. در نهایت، رویکردهای پاتولوژیک جدید مثل طبقهبندی PitNET نگاه عمیقتری به رفتار زیستی این تومورها میدهد و زمینه را برای درمانهای هدفمندتر فراهم میکند.